Metallernes atomare struktur og tilstandsformer
|
|
|
- Valdemar Graversen
- 7 år siden
- Visninger:
Transkript
1 Metallernes atomare struktur og tilstandsformer Metallernes struktur, opbygning og tilstandsformer For at få en forståelse af metallernes særlige måde at opføre sig på i forhold til andre materialer, er det nødvendigt, at man har et kendskab til, hvordan materialerne er opbygget, helt fra den mindste bestanddel, atomet, og op til det samlede produkt: det emne, vi skal bearbejde. Vi kan som udgangspunkt se på en stålklods og hurtigt arbejde os ned til atomet og derfra på tilbagevejen prøve at se på det, vi møder, og prøve at få et overblik og lidt orden i det, vi møder på vejen. Atomets opbygning Når vi ser på en stålklods, ser den ud som et stort samlet materiale. Det er dog ikke tilfældet. Hvis vi ser det samme materiale under et mikroskop, vil vi i den blanke overflade kunne se, at materialet er sammensat af mange små korn, eller, som det også kaldes, krystaller. Når vi ser på materialernes egenskaber, bestemmes de oftest af de elektroner, der sidder i den yderste bane eller skal, som det også kaldes, men inden vi går videre med dette, må vi nok lige se på, hvordan et atom er sammensat. Til forklaring af atomet kan vi anvende vor landsmand Niels Bohrs atommodel, der forenklet ser ud på følgende måde: Selve atomkernen består af protoner og neutroner, der har fællesbetegnelsen nucleoner. Protonen er elektrisk positiv, neutronen er elektrisk neutral. Den væsentligste del af atomets masse findes i atomkernen, antallet af protoner er det, der giver grundstoffet eller atomet sit nummer i rækken af grundstoffer, atomnummeret har betegnelsen Z. Omkring atomkernen kredser der et antal elektroner, der har en negativ ladning. Elektronernes antal svarer til det antal postitivt ladede protoner, der er i atomkernen. ma tif Metalkorn Kunne vi nu finde et mikroskop, der kunne forstørre mange flere gange, ville vi nok kunne se materialets mindste bestanddele, nemlig atomerne. ma cdr Atomkerne Det samlede atom vil derved udadtil virke elektrisk neutralt, hvis det får lov til at være upåvirket af andre atomer, der kan omdanne det til en ion, hvilket kan ske, hvis der fjernes eller tilføres en eller flere af de yderste elektroner, der også kaldes valenselektroner. ma cdr Atom 1
2 ma cdr Når antallet af elektroner i skal når otte, begynder atomet at fylde en ny skal op. Når fjerde til syvende skal fyldes, starter opfyldningen i hovedgrupperne IA og IIA med to elektroner, før den foregående skal fortsættes med opfyldningen. Det videre forløb af opfyldningen, når vi er nået til metallerne, er et større område, se derfor efterfølgende tabel over grundstofferne. Dette, at skallen fyldes op til otte elektroner, der i øvrigt synes at gøre atomet særlig stabilt, kaldes oktetreglen. Atomer med otte elektroner i yderste skal kaldes ædelgasser. Fælles for de fleste metaller er, at de har to eller færre løstsiddende elektroner i yderste skal, se senere. Når vi skal have et overblik over atomerne eller grundstofferne, kan det gøres ved at ordne dem efter stigende atomnummer. Den orden, de vil fremkomme i, kaldes det periodiske system. 2 Industriens Forlag - Ma170.fm
3 Det periodiske system For at danne sig et overblik over atomerne/ grundstofferne er det nødvendigt at sætte tingene lidt i system. Det startede man på i ca. år 1800, hvor man kendte ca. 30 grundstoffer, og til i dag, hvor man kender 110 grundstoffer. En del af de sidste, fra nr. 95 til 110, fremstilles i laboratorier og er kun stabile et kort øjeblik. Som vi omtalte under metallernes struktur, er det periodiske system ordnet efter atomnummer, det vil derfor fremstå som nedenstående model af det periodiske system. Når vi ser på modellen nederst, vil vi se, at den er inddelt med otte lodrette hovedgrupper mærket med A og 10 undergrupper mærket med B. Ser man på en hovedgruppe, svarer antallet af elektroner i den yderste skal til hovedgruppens nummer. Undtaget er He, der er stabil med to elektroner og derfor står sammen med de stabile i 8 hovedgrupper. I undergrupperne er dette desværre ikke altid tilfældet. Den vandrette inddeling sidegruppeinddelingen fortæller, hvor mange skaller atomet har. Man kan fra tabellen se, at der er maks. 7 skaller i hele atomsystemet. Ud fra det periodiske system kan vi uddrage mange forskellige oplysninger, f.eks. at vægten er stigende, hvilket kan ses af atommassen, se på jern, hvor atommassen er 55,8, og kobber med atommasse på 63,6 samt, hvis systemet indeholder en elektronnegativitetstabel, også, hvilken bindingstype der vil fremkomme ved en evt. legering. Dette er oplysninger, der har interesse ved fremstillingen af materialerne, da det har indflydelse på styrken i materialerne. Vi har nu set på, hvordan atomerne er opbygget, og i hvilken orden de er placeret, og vil nu se på, hvordan de opfører sig over for hinanden, når de binder sig sammen, og hvilken betydning det har for os, når vi skal bruge dem. Lithium (Li) og natrium (Na) har altså begge en elektron i yderste skal, og ilt (O) nr. 8 og svovl (S) nr. 16 har begge seks elektroner i den yderste skal. ma cdr Det periodiske system 3
4 Tabel over grundstofferne er sjældne jordarters metaller. Elektronstruktur Nr. Navn Symbol Atomvægt skal 1 Hydrogen (Brint) H 1, Helium He 4,0 2 3 Lithium Li 6, Berylium Be 9, Bor B 10, Kulstof (Carbon) C Kvælstof (Nitrogen) N Ilt (Oxygen) O Fluor F Neon Ne Natrium Na Magnesium Mg 24, Aluminium Al Silicium Si Fosfor (Phosphor) P Svovl S Klor (Chlor) Cl 35, Argon A Kalium K Calcium Ca Scandium Sc Titan Ti Vanadium V Chrom Cr Mangan Mn Jern Fe 55, Kobolt Co 58, Nikkel Ni 58, Kobber Cu 63, Zink Zn Gallium Ga Germanium Ge 72, Arsen As Selen Se Brom Br Krypton Kr Rubidium Rb Strontium Sr Yttrium Y Zirkon Zr Niobium (Columbium) Nb Molybdæn Mo Tecnetium Tc Ruthenium Ru Rhodium Rh Industriens Forlag - Ma170.fm
5 Elektronstruktur Nr. Navn Symbol Atomvægt skal 46 Palladium Pd Sølv Ag Cadmium Cd Indium In Tin Sn Antimon Sb Tellur Te Iod I Xenon Xe Cæsium Cs Barium Ba Lanthan La Cerium Ce Praseodym Pr Neodym Nd Promethium Pm Samarium Sm Europium Eu Gadolinium Gd Terbium Tb Dysprosium Dy Holmium Ho Erbium Er Thulium Tm Ytterbium Yb Lutetium Lu Hafnium Hf Tantal Ta Wolfram (Tungsten) W Rhenium Re Osmium Os Iridium Ir Platin Pt Guld Au Kviksølv Hg Thallium Tl Bly Pb Wismut (Bismuth) Bi Polonium Po Astat At Radon Rn Francium Fr Radium Ra Actinium Ac Thorium Th Protactinium Pa Uran U
6 Elektronstruktur Nr. Navn Symbol Atomvægt skal 93 Neptunium Np Plutonium Pu Americium Am Curium Cm Berkelium Bk Californium Cf Einsteinium Es Fermium Fm Mendelevium Md Nobelium No Lawrencium Lr Tilstandsformer De fleste materialer og alle metaller, vi kender, kan forekomme i de tre kendte tilstandsformer: Fast form, også kaldet fast fase Flydende form, også kaldet væskefase Luft form, også kaldet damp eller gasfase Disse tre tilstandsformer gennemgår de fleste kendte metaller, når de påvirkes af forskellige temperaturer. Ser vi på et materiale, vi kender fra vor dagligdag, rent jern uden tilsætningsstoffer, vil vi se, at det har fast/flydende form indtil ca C, hvor det smelter, hvorefter det ved C, går over i gasfasen. Temperaturen, hvor ændringerne sker, kan ændres, når det atmosfæriske tryk ændres, ovenstående temperatur er f.eks. gældende ved 1 atmosfæres tryk. Ved stigende tryk falder temperaturen for faseskiftene. Denne egenskab er baggrunden for, at man i stor udstrækning benytter væske under tryk til køling af forbrændingsmotorer. Ved at hæve trykket i kølesystemet til 1,4 bar kan temperaturen hæves til 120 C, uden at systemet koger over. Fænomenet udnyttes ligeledes i trykkogere, hvor tilberedningstiden for f.eks. en portion kartofler kan reduceres ved, at man opvarmer vandet til omkring 110 C. Når et materiale er i de forskellige faser, er sammenholdet/bindingen mellem de enkelte atomer også forskellig. ma cdr Faseændring I gasfasen er der ingen eller kun svag binding mellem atomerne, hvilket vil bevirke, at materialet hurtigt spredes, hvis det ikke er i en lukket beholder. Når materialet går fra gas til flydende fase, bliver afstanden mellem atomerne mindre, og de tiltrækkes mere til hinanden, men kan dog stadig bevæge sig indbyrdes. I den faste fase er atomerne stoppet med at bevæge sig indbyrdes, men har dog stadig en vis aktivitet i elektroner. Den måde, atomerne placerer sig på ved størkningen, kaldes krystalgitre. Ethvert materiale har sit eget krystalgitter, der er en vigtig del af materialets egenskab. Når et materiale skal til at danne et krystalgitter, starter det med, at atomerne begynder at søge sammen, eller som det kaldes, at binde sig til hinanden. 6 Industriens Forlag - Ma170.fm
7 De materialer, vi anvender i vor dagligdag, har tre primære bindingstyper, de sekundære vil ikke blive omtalt her: Ion-binding Kovalent-binding Metal-binding Lad os se på, hvordan og hvorfor de binder sig, som de gør. Som omtalt tidligere, vil atomerne, når materialerne skifter fase, begynde at nærme sig hinanden. Når dette sker, vil de positive ioner tiltrække de negative på samme måde, som når man sætter to magneter over for hinanden. Vender man magneterne, vil de frastøde hinanden. Tilsvarende vil ske, når positive og negative partikler møder hinanden. Atomerne bliver derved til positive og negative ioner, der vil tiltrække hinanden som magneterne. Ion-binding er en meget stærk bindingstype, der kan opstå mellem to grundstoffer, ofte mellem et metalatom og et ikke-metalatom, f.eks. i keramiske materialer. Materialer med overvejende ionbinding har en stor hårdhed og stivhed, dermed følger desværre også, at materialet er skørt. Årsagen skal findes i den måde, bindingen samles på, når det opbygger sit krystalgitter. Ion-gitteret holdes som omtalt sammen ved hjælp af ionernes positive og negative ladninger. Når disse bindinger overbelastes (brydes), vil de, da de ligger med negative ioner over positive, som magneterne vi omtalte tidligere, frastøde hinanden og vil ikke gendannes. Materialet er dermed brudt. Positiv ion Negativ ion ma cdr Den måde, atomerne/ionerne finder sammen på (bindingstyperne), skyldes, at grundstoffernes forskellige elektriske opbygning af atomer har forskellig elektron-negativitet. Lad os på denne baggrund se på de forskellige bindingstyper. Ion-binding Ved ion-binding forærer det ene atom en eller flere elektroner til et andet atom. ma cdr Ion-gitter ma cdr + Ion-binding Kovalent-binding Ved den kovalente binding sker der som ved ionbindingen også noget med de yderste elektroner, valenselektronerne. Ved ion-bindingen afgav eller modtog de forskellige atomer elektroner og blev dermed enten positive eller negative. Ved kovalent-binding deles man om de valenselektroner, man har, i almindeligt fælleseje, f.eks. har siliciumatomet, som kan findes i fjerde hovedgruppe i det periodiske system, fire elektroner i sin yderste skal. 7
8 Den vil kunne binde sig med andre siliciumatomer, således at oktetreglen opfyldes. Metal-binding Den bindingsform, vi oftest møder i vort daglige arbejde med vore materialer (metallerne), er naturligvis metal-binding. Ved metal-binding er der ikke som ved ion- og kovalent-binding udveksling eller deling af valenselektronerne. Metal-bindingens elektroner danner nærmest en fælles negativ elektronsky omkring metalionerne, se tegning, og vil derved holde de nu positive metalioner på plads i krystalgitteret. ma cdr Silicium (Si) Oktetreglen kan også opfyldes med f.eks. klor, der har syv valenselektroner. ma cdr Metal-binding Da elektronskyen ikke er bundet fast til et eller flere atomer, er det muligt at bevæge de enkelte atomer hen over hinanden (i slipplanerne), mens de stadig er fastholdt af elektronskyen. ma cdr Klormolekyle Kovalent-bindinger er meget stærke, men også meget sprøde. Årsagen skal også her findes i krystalgitteret, hvor vi ser, at atomerne skal rives ud af deres binding med hinanden og vil, når bindingerne er brudt, ikke gendannes. Kovalentbindinger finder vi i keramiske materialer, hvor de er bundet i krystalgitre samt i polymerer, hvor de findes i lange kæder, hvis det er termoplastiske materialer, og som et krystal, når det er hærdeplast. Materialer med metal-binding er seje og lader sig gerne bearbejde ved bukning og strækning eller presning. De materialer, vi møder i dagligdagen, er ikke rene materialer, grundstoffer, men vil indeholde forskellige tilsætningsstoffer. Dette bevirker, at vi i de fleste materialer vil finde to eller tre af de ovenstående bindinger i større eller mindre grad. 8 Industriens Forlag - Ma170.fm
9 Krystalstrukturer Atomer, der samler sig i ideale og fejlfrie metaller, vil danne bestemte mønstre, krystalgitre, der vil være ens i alle retninger i det enkelte krystalkorn. Vi vil til dette anvende nogle modeller, hvor atomerne optræder som lige store kugler. Materialer, der samler sig i faste mønstre, kaldes krystallinske. Materialer, der samler sig uden bestemte mønstre, kaldes amorfe (uden form), dette kan f.eks. være visse plast- og keramiske materialer. Simpel kubisk Kubisk fladecentreret Kubisk rumcentreret Metalmaterialernes krystallinske opbygning Simpel tetragonal Rumcentreret tetragonal Hexagonal Simpel ortorombisk Rumcentreret ortorombisk Grundcentreret ortorombisk Fladecentreret ortorombisk ma cdr Metallerne ordner sig i gitterform Formen af gitteret og materialets renhed har stor betydning for de egenskaber, sejhed m.m., materialet får, når det skal anvendes. Den form eller gitterstruktur, materialerne har, ser vi bedst ved at se på den mindste del af mønsteret, der f.eks. kan have form som en terning, eller, som det kaldes, enhedscellen. Enhedscellen er det mindste antal atomer, der danner krystallets symmetri, f.eks. en terning eller en kubus, som det også kaldes. Enhedscellen er for metallerne en meget enkel opbygning. Rombehedralsk ma cdr Simpel monoklinsk Grundcentreret monoklinsk De syv krystalsystemer Triklinsk Hexagonal gitterstruktur Den hexagonale enhedscelle vil se ud som nedenstående tegning. Cellen har i alt 17 atomer, hvoraf den deler de 14 med nabocellerne, numrene 4 til 17, når cellen sidder i sin gitterstruktur. Der findes syv krystalsystemer med i alt 14 enhedsceller, se efterfølgende tegning. Vi har inden for metallerne normalt kun brug for fire af enhedscellerne: Hexagonal gitterstruktur Tetragonal gitterstruktur Kubisk rumcentreret gitterstruktur Kubisk fladecentreret gitterstruktur Vi ser på gitterstrukturerne en ad gangen, hvordan de er bygget op, og i hvilke materialer de kan findes. ma cdr Hexagonal kuglepakning 9
10 Af de mest almindelige metaller med denne struktur kan nævnes zink, magnesium, titan og kobolt. Tetragonal gitterstruktur Den tetragonale gitterstruktur har facon som en lidt fladtrykt eller langstrakt terning. Cellen har i sin simpleste grundform otte hjørneatomer, som den deler med nabocellerne i gitterstrukturen. Den fladecentrerede enhedscelle er tættere pakket end den rumcentrerede, hvilket bl.a. er en af årsagerne til, at jern over 910 C som austenit er lettere at strække og bøje. ma cdr Fladecentreret kuglepakning Af materialer med denne struktur kan nævnes jern over 910 til C, nikkel, aluminium, kobber, bly, guld, sølv og mange andre metaller. ma cdr Tetragonal kuglepakning Den tetragonale struktur findes i tin, bor, radium og hærdet stål. Kubisk rumcentreret gitterstruktur Den kubiske rumcentrerede enhedscelle har facon som en almindelig terning, hvor der er et atom i hvert hjørne samt et atom i midten. Når vi her har set tæt på, hvordan enhedscellerne og gitterstrukturen er i de forskellige materialer, skyldes det, at nogle af metallernes egenskaber er knyttet til disse opbygninger. En vigtig del af egenskaberne er materialernes evne til at lade sig forme ved tryk eller træk, også kaldet den plastiske deformationsevne, hvis årsag bl.a. skal findes i enhedscellernes slipplaner. Slipplaner eller atomplanglidning ma cdr Rumcentreret kuglepakning Denne enhedscelle findes i jern op til 910 C og fra C til smelte, endvidere findes den hos molybdæn, wolfram og chrom. Kubisk fladecentreret gitterstruktur Den kubiske fladecentrerede enhedscelle har også facon som en terning med et atom i hvert hjørne, men har endvidere et atom på hver flade. Dette giver otte hjørneatomer og seks fladeatomer, i alt 14 atomer, se tegning, som alle deles med nabocellerne. Trækker eller trykker man i et materiale med en ikke for stor kraft, vil alle materialer være elastiske. Elasticiteten vil vare, indtil atombindingerne brydes, og der ved hårde materialer med primære kovalent-bindinger, f.eks. glas og keramiske materialer, sker brud, eller som ved metaller, hvor der vil ske atomplanglidninger i slipplanerne, hvorved metallet får en plastisk deformation. En jernstang, der bøjes, får en plastisk deformation med både træk og trykspændinger. Den kraft, der skal til at forme forskellige metaller, er afhængig af den tæthed, der er i gitterstrukturens kuglepakning. Er kuglepakningen meget tæt, vil kuglerne kunne glide let mellem hinanden og skal ikke bruge stor kraft til at løfte de modstående atomlag fra hinanden. Det modsatte er tilfældet, når kuglepakningen er løs. 10 Industriens Forlag - Ma170.fm
11 Slipplan Slipretning ma cdr Deformationen sker trinvis ved relativ glidning mellem to atomanlæg Om kuglepakningen er tæt eller løs, samt hvilke retninger (slipplaner) atomerne kan glide i, kan vi se af enhedscellernes opbygning. Slipplanerne ligger i de planer i elementarcellerne, hvor kuglepakningen er tættest. Slipplanerne i de tre mest forekommende enhedsceller er her tegnet. Den hexagonale enhedscelle har tre slipretninger, der alle ligger i samme slipplan. Deformation af hexagonale materialer kan dog være vanskelig trods den tætte kuglepakning. Dette skyldes, at det kan være vanskeligt at ramme et enkelt slipplan med kraftpåvirkningen. Slipplan ma cdr Kubisk fladecentreret gitter Den kubisk rumcentrerede enhedscelle har 12 ikke parallelle slipplaner og en løsere kuglepakning, der vil kræve en større kraftpåvirkning end den fladecentrerede, når der skal deformeres materiale med denne struktur, jf. tidligere. At glideplaner har stor indflydelse på, hvor meget og hvor lidt et materiale kan deformeres, kan vi se af, at magnesium med hexagonalt gitter skal anvende ca. 100 N/mm 2 for at lave den maks. forlængelse, materialet har på ca. 10 til 15%. Aluminium med kubisk fladecentreret gitter skal derimod bruge 25 N/mm 2 for at få sin maks. forlængelse på ca. 50%. De slipplaner, vi har set indtil nu, har været i perfekte krystalgitre. I virkeligheden vil de fleste af de materialer, vi anvender, indeholde forskellige former for fejl, som vi skal se i følgende afsnit. Slipretning Slipplan Slipretning ma cdr Hexagonalt gitter Den kubisk fladecentrerede enhedscelle er med sine 24 ikke parallelle slipplaner den letteste at deformere. Dette skyldes, at cellen har en tæt kuglepakning, der sammen med de mange slipplaner gør, at den kraft, der skal anvendes, får mange muligheder for at ramme et slipplans retning. ma cdr Kubisk rumcentreret gitter Gitterfejl Gitterfejl De mest almindelige former for fejl i atomgitteret er punktfejl og liniefejl. Fejlene opstår, når materialerne starter med gitteropbygningen, ved overgangen fra flydende til fast form, ved tilsætning af legeringsmaterialer eller ved en senere deformation, varmebehandling, svejsning, hærdning m.m. Fejlene har betydning for materialernes egenskaber, hvilket vi kan se af følgende. 11
12 Punktfejl De oftest forekommende punktfejl er: Små eller store fremmede atomer fra legeringsmaterialer, der optager et af grundmetallets atomers plads i gitteret. Disse kaldes substitutionsatomer Små atomer kan til tider finde plads mellem atomerne i gitterstrukturen uden at optage pladsen fra et af grundmaterialets atomer. Disse kaldes indskudsatomer Der kan også opstå den fejl, at der mangler et atom i gitteropbygningen. Det vil bringe forstyrrelse i det omkringliggende gitter, men kan dog også være til hjælp, når der sker diffusion mellem atomerne i materialet. Denne fejltype kaldes vakance Liniefejl Liniefejl, også kaldet dislokationer, er en fejl i gitterstrukturen, der går gennem (hele) krystallet. Dislokationen optræder som et ekstra atomplan i en ellers perfekt gitterstruktur. ma cdr Krystaller kan have gitterfejl som f.eks. indskudsatomer eller dislokationer ma cdr Punktfejl i metalgitteret Dislokationer er til stor hjælp ved deformation af materialer. Kantdislokation, som vi omtaler her, vil let kunne bevæge sig gennem atommønsteret i slipplanerne ved en kraftpåvirkning udefra, f.eks. træk eller tryk. Den»tomme«plads vil løbe som en bølge gennem krystallet, til den når kanten af krystallet eller korngrænsen, se tegningen, hvorefter dislokationen vil ophøre. I et udeformeret materiale er der op til ca dislokationer pr. cm 2. Når et materiale er blevet deformeret, f.eks. bukket, vil der opstå en del nye dislokationer, helt op til gange så mange som fra begyndelsen. Da en del af de nu opstående dislokationer krydser hinanden, vil de låse hinandens bevægelser, og materialet bliver stift. Dette vil man kunne mærke, når man forsøger at rette en bøjet metalstang til lige igen. Ser vi på de to første gitterfejl, vil de være en hindring for de slip, der kan foretages på slipplanerne. Der skal anvendes større kraft for at deformere materialer med denne fejltype. Tilsætning af substitutionsatomer foretages ofte i metaller som legeringsmaterialer, da de giver grundmaterialet nye og anderledes egenskaber, styrke m.m. Den tredje fejl må anses for at være en fordel for deformation, da den letter atomerne, når de skal bytte plads, f.eks. ved bukning, varmebehandling m.m. ma cdr Dislokationsvandring ved deformation Der er på denne måde sket en deformationshærdning, som øger styrken i metallet. Deformationshærdning anvendes til at forbedre styrken i f.eks. kobber og aluminium, der ikke kan hærdes på anden vis, samt til øgning af almindeligt billigt stål som armeringsjern til betonkonstruktioner, tentorstål m.m. 12 Industriens Forlag - Ma170.fm
13 Vi har nu set, hvordan atomerne er opbygget, og hvordan de samler sig i mere eller mindre perfekte systemer. Vi vil nu se på, hvordan metallerne samler sig fra flydende til størknet materiale. Mikrostrukturer Når metaller går fra smeltet til fast materiale, vil det ved normal afkølingshastighed størkne som en mængde uregelmæssige metalkorn. Korndannelsen vil starte mange steder i det smeltede materiale ved opbygning af enhedsceller, der vil danne en gitterstruktur, som under rolige forhold vil udvikle sig i alle retninger i det smeltende materiale. De forskellige gitre vil under udviklingen mødes, men vil ikke kunne samles til et hele, da gitrene mødes fra forskellige retninger. Det sted, gitrene mødes, vil til slut danne korngrænserne. Kornstørrelsen har betydning for materialets styrke, således at finkornet materiale har større styrke end grovkornet. Det er muligt at være medbestemmende på kornenes størrelse ved afkølingen af materialet. Køles materialet hurtigt, vil det blive finkornet, dvs. at kornene bliver mindre end ca. 0,01 mm i udstrækning. Ved almindelig, rolig afkøling i fri luft bliver kornstørrelsen i stål normalt ca. 0,10 mm. Den her omtalte korndannelse fra smeltet til størknet materiale kan delvis også foregå i udelukkende størknet materiale og kaldes rekrystallisation. Rekrystallisation anvendes, når et materiale er blevet deformationshærdet. Ved rekrystallisationsglødning søger man at gengive materialet sine oprindelige egenskaber ved at fjerne det store antal dislokationer, der er opstået ved kolddeformationen. For at opnå et godt resultat ved rekrystallisationsglødningen skal materialet have en deformationsgrad på mere end 20 til 25% varierende for forskellige metaller. Er deformationsgraden mindre, kan materialet blive grovkornet i stedet. Rekrystallisationstemperaturen og holdetider omtales under varmebehandling. Tilstandsdiagrammer Vi ved nu, at materialer kan forekomme i forskellige tilstande, fast, flydende og gasform. Endvidere kan der inden for samme tilstandsform forekomme forskellige strukturer (faser), som f.eks. jern over 910 C med kubisk fladecentreret krystalgitter og under med kubisk rumcentreret gitter. Ved at blande, legere, materialer vil man ofte kunne opnå nye egenskaber, f.eks. større styrke m.m. ma cdr Skematisk fremstilling af en krystallisation For let at kunne overskue, hvordan et blandet materiale vil opføre sig ved forskellige temperaturer, kan man opbygge et fase- eller tilstandsdiagram. Et meget brugt fasediagram er jernkulstofdiagrammet, som vi skal se på senere, men først lidt om, hvordan et fasediagram bliver opbygget. 13
14 Udarbejdselsen af fasediagrammer foregår ved hjælp af smeltepunkter eller smelteintervaller og afkølingskurver. Som vi husker fra naturlæren, vil et diagram for f.eks. vand se ud som denne tegning. I legerede materialer er der intet smeltepunkt, men et smelteinterval, hvor der forekommer smeltet materiale og fast materiale på en gang, selv om der fortsat tilføres energi. C Afkøling ma cdr Opvarmningskurve for H 2 O ma cdr Størkning/smelte Størknings/ smelteinterval Fast materiale Begyndende størkning kaldet liquidus = L Størkningen afsluttet kaldet solidus = S Opvarmnings/afkølingskurve for 30% nikkel og 70% kobber Energi Som vi må huske, er der i rene materialer et smeltepunkt, altså ingen temperaturstigning i materialet, før alt er omdannet til den nye tilstandsform, selv om der fortsættes med tilførsel af energi. Ved at udarbejde et større antal forskellige kurver med forskelligt indhold af de ønskede legeringsmaterialer (her Ni og Cu) kan man fremstille et fasediagram, der dækker et helt område for de ønskede legeringer. 14 Industriens Forlag - Ma170.fm
15 Nikkel/kobber-diagrammet er et meget enkelt diagram, hvor der kun findes få faser. Der er fuldstænding opløselighed mellem Ni- og Cukrystallerne, de er blandingskrystaller. Et noget mere kompliceret diagram er jern-kulstofdiagrammet. I dette diagram forekommer der nemlig flere faser, både blandingskrystaller og krystaller, der er opbygget af den kovalente forbindelse, (Fe 3 C) samt flydende og faste faser. Opbygningen af dette diagram foretages også for bestemmelse af fasernes beliggenhed ved hjælp af afkølingskurver. Kendskab til jern-kulstofdiagrammet har stor betydning i vort fagområde, både til hærdning og ved svejsning m.m. Vi skal derfor prøve at se på opbygningen af dette fasediagram. Anvendelse af diagrammet til varmebehandling omtales under afsnittet»varmebehandling«. Til at belyse jern-kulstofdiagrammet vil vi tage udgangspunkt tre steder (0,0% C, 1,0% C og 3,5% C) i det store jern-kulstofdiagram. Dette dækker området fra 0 til 7% C, selv om jern med mere end 5% C er uanvendeligt. Det lille jernkulstofdiagram går fra 0,0 til 2,05% C og dækker det område, vi kender fra ulegeret stål. Ved afkøling af jern med 0,0% C fra C vil vi få følgende faser: Ved området fra til C vil det rene jern være flydende og uden fast gitterstruktur. Fra og til C vil jernet have dannet krystalgitter med en kubisk rumcentreret enhedscelle, jernet kaldes her deltajern. Ved og til 912 C omdannes det omtalte delta-jern til gamma-jern eller austenit, som det også kaldes, med en kubisk fladecentreret enhedscelle. Fra 912 C og til 0,0 C har jern igen en kubisk rumcentreret enhedscelle, jernet kaldes nu alphajern. Det rene jern har altså mange forskellige faser, disse har endvidere forskellige egenskaber. En af de vigtigste egenskaber er fasernes evne til at optage f.eks. kulstof ved forskellige temperaturer. Starter vi med at se på delta-jern, kan det højst have 0,08% C opløst ved C, se pkt. A. Gamma-jern kan højst have en opløsning på 2,05% C ved C, se pkt. E. Alpha-jern kan højst have 0,025% C ved 723 C, se pkt. C. Med disse opløsningsprocenter må en rest kulstof blive omdannet til noget andet. Lad os prøve at tage et jernmateriale med 1,0% C og samme temperaturforløb og se, hvilke ændringer der sker med materialet. 15
16 Jern med 1,0% C vil ved C være flydende ned til C. Som man kan se, vil kulstofindholdet bevirke, at der sker en sænkning af temperaturen, hvor jernet begynder at størkne. Fra og til C vil jernet bestå af austenitkrystaller og smeltet materiale. Ved C vil jernet være størknet og have austenitisk krystalstruktur. Denne struktur vil jernet have, til det kommer lidt under S-E linien ved 790 C. Fra 790 og ned til 723 C vil der i austenit-korngrænserne dannes en ny struktur, kaldet cementit. Denne krystalstruktur er ortorombisk og er altså en ny krystalstruktur. Cementit er jernkarbid med kovalent binding, der er meget hård og sprød. Den kemiske sammensætning er Fe 3 C, der skal altså anvendes tre jernatomer og et kulstofatom for at danne denne struktur. Cementitten har ved alle temperaturer, hvor den forekommer, et bestemt kulstofindhold på 6,68% C. Man kan se, at det netop bliver denne kulstofprocent ved følgende regnestykke. Fra den kemiske sammensætning så vi, at cementit bestod af tre jernatomer og et kulstofatom. Finder vi atommassen i grundstoftabellen (Det periodiske system), ser vi, at jern Fe har atommassen 55,8 og kulstof C har atommassen 12,00. Den samlede atommasse bliver derved for 3 stk. Fe og 1 stk. C: 3 55,8 + 12,00 = 179,4. Ved almindelig procentregning ser vi, at kulstoffet udgør: 12, , 4 = 6,688% af den samlede atommasse. Ved passagen af linien C-K og ned vil den austenit, der ikke er omdannet til cementit, have et kulstofindhold på 0,8% C. Jern med dette kulstofindhold vil, når det kommer under 723 C, omdannes til en ny struktur, der kaldes perlit. Perlitten har på grund af sin struktur, der skiftevis i lagene er det meget bløde Fe og meget hårde og skøre Fe 3 C, en god trækstyrke, men en lille sejhed. Et stål, som vi her ser på med 1% C, vil derfor være vanskeligt at bearbejde. Da perlitiske stål dog har mange gode egenskaber, leveres de ofte i en anden struktur fra stålværkerne, strukturen kaldes sfærodiseret. Varmebehandlingen til denne struktur omtales under varmebehandling. Det sidste materiale, vi ser på i dette tilstandsdiagram, er jern med 3,5% C og er altså et materiale uden for det lille jern-kulstofdiagram, der kun går op til ca. 2,05% C. Jern fra 2,05 og op til 5% C kaldes støbejern. Vi vil igen starte ved C og gå ned til stuetemperatur. Materialet vil fra og til C være i flydende form, her er der virkelig sket en sænkning af størkningspunktet, som kan ses. Når vi passerer linien ved de C, begynder jernet at størkne. Det smeltede materiale vil begynde at udskille austenitkrystaller, som indeholder maks. 2,05% C. Den overskydende mængde kulstof vil blive mere og mere koncentreret i den resterende mængde smeltet materiale. Ved overskridelse af E-F-linien er alt materialet størknet, dels som austenitkrystaller, af hvilket der vil være flest, og dels som en blanding af cementit- og austenitkrystaller. Ved fortsat afkøling vil austenitten omdannes til perlit og cementit. Som vi tidligere har set, var cementitten hård og skør, og perlitten var også hård og dårlig at bearbejde med almindeligt værktøjsstål. Vi må derfor antage, at materiale med 3,5% C er vanskeligt at bearbejde ved almindelig skærende bearbejdning og bearbejdes da også oftest kun ved slibning. Materialet kan dog ændres ved specielle varmebehandlinger, så bearbejdningen gøres lettere. Dette ser vi på i afsnittet om varmebehandling. Perlitten består af Fe og Fe 3 C. Perlitstrukturen er en lagdelt struktur, således at forstå, at den danner plader skiftevis af Fe og Fe 3 C. Ser man på en perlitstruktur under et mikroskop, kan strukturen ligne et fingeraftryk, hvor stregerne skiftevis er Fe- og Fe 3 C-lameller. 16 Industriens Forlag - Ma170.fm
17 Data for enkelte grundstoffer Navn Krystalgitter Symbol Smeltepunkt C Kogepunkt C Massefylde g/cm 3 Atomdiameter Å Aluminium Al Kubisk fladecentreret ,7 2,86 Antimon Sb Rombohedralsk 630, ,68 2,92 Barium Ba Kubisk rumcentreret ,5 4,35 Berylium Be Hexagonal ,82 2,23 Bly Pb Kubisk fladecentreret ,34 3,50 Bor B Tetragonal ,6 1,98 Brint (hydrogen) H Hexagonal ~ 0,92 Cadmium Cd Hexagonal ,65 2,98 Calcium Ca Kubisk fladecentreret ,55 3,94 Cerium Ce Kubisk fladecentreret ,77 Fosfor (phosphor) P Rombohedralsk ,83 2,88 Guld Au Kubisk fladecentreret ,3 1,32 Ilt (oxygen) O ~ ~ 2,71 Iridium Ir Kubisk fladecentreret ,5 2,48 Jern Fe Kubisk rumcentreret (kubisk ,87 2,55 fladecentreret) Kobber Cu Kubisk fladecentreret ,96 2,52 Kobolt (cobolt) Co Kubisk fladecentreret og ,9 1,82 hexagonal Chrom Cr Kubisk rumcentreret ,19 2,50 Kulstof (diamant) C Kubisk ,51 1,54 Kulstof (grafit) C Hexagonal ~ ~ 2,20 1,54 Kviksølv Hg Rombohedralsk ,55 3,00 Kvælstof (nitrogen) N ~ ~ 1,42 Magnesium Mg Hexagonal ,74 3,20 Mangan Mn Kubisk ,43 3,20 Molybdæn Mo Kubisk rumcentreret ,2 2,72 Nikkel Ni Kubisk fladecentreret ,90 2,44 Niobium (columbium) Nb Kubisk rumcentreret ,57 ~ Platin Pt Kubisk fladecentreret ,45 2,77 Silicium Si Kubisk ,33 2,35 Svovl S Rombohedralsk ,05 2,85 Sølv Ag Kubisk fladecentreret ,5 2,88 Tantal Ta Kubisk rumcentreret ,6 2,86 Tellur Te Hexagonal ,24 2,74 Tin Sn Tetragonal ,30 3,02 Titan Ti Kubisk rumcentreret og ,51 2,94 hexagonal Uran U Ortorombisk ,76 Vanadium V Kubisk rumcentreret ,63 Wismut (bismuth) Bi Rombohedralsk ,8 3,11 Wolfram (tungsten) W Kubisk rumcentreret ,3 2,74 Zink Zn Hexagonal 419, ,14 2,66 17
Opgaver i atomer. c) Aflæs atommassen for Mg i det periodiske system eller på de udskrevne ark, og skriv det ned.
 Opgaver i atomer Opgave 1 Tegn atomerne af nedenstående grundstoffer på samme måde, som det er vist for andre atomer i timen. Angiv protoner med plusser. Vedrørende elektroner: Husk, at der maksimalt kan
Opgaver i atomer Opgave 1 Tegn atomerne af nedenstående grundstoffer på samme måde, som det er vist for andre atomer i timen. Angiv protoner med plusser. Vedrørende elektroner: Husk, at der maksimalt kan
DET PERIODISKE SYSTEM
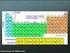 DET PERIODISKE SYSTEM Tilpasset efter Chemistry It s Elemental! Præsentation fra the American Chemical Society, Aug. 2009 http://portal.acs.org/portal/publicwebsite/education/outreach/ncw/studentseducators/cnbp_023211
DET PERIODISKE SYSTEM Tilpasset efter Chemistry It s Elemental! Præsentation fra the American Chemical Society, Aug. 2009 http://portal.acs.org/portal/publicwebsite/education/outreach/ncw/studentseducators/cnbp_023211
Vikar-Guide. Den elektriske ladning af en elektron er -1 elementarladning, og den elektriske ladning af protonen er +1 elementarladning.
 Vikar-Guide Fag: Klasse: OpgaveSæt: Fysik/Kemi 9. klasse Atomernes opbygning 1. Fælles gennemgang: Eleverne skal løse opgaverne i små grupper på 2-3 personer. De skal bruge deres grundbog, og alternativt
Vikar-Guide Fag: Klasse: OpgaveSæt: Fysik/Kemi 9. klasse Atomernes opbygning 1. Fælles gennemgang: Eleverne skal løse opgaverne i små grupper på 2-3 personer. De skal bruge deres grundbog, og alternativt
Atomets bestanddele. Indledning. Atomer. Atomets bestanddele
 Atomets bestanddele Indledning Mennesket har i tusinder af år interesseret sig for, hvordan forskellige stoffer er sammensat I oldtiden mente man, at alle stoffer kunne deles i blot fire elementer eller
Atomets bestanddele Indledning Mennesket har i tusinder af år interesseret sig for, hvordan forskellige stoffer er sammensat I oldtiden mente man, at alle stoffer kunne deles i blot fire elementer eller
Naturfag. Supplerende materiale. 5. udgave
 Naturfag Supplerende materiale 5. udgave Uorganisk kemi Uorganisk kemi Atomets opbygning - en teori Alle ting omkring os, uanset form, farve og størrelse, er opbygget af bittesmå partikler. De kan ikke
Naturfag Supplerende materiale 5. udgave Uorganisk kemi Uorganisk kemi Atomets opbygning - en teori Alle ting omkring os, uanset form, farve og størrelse, er opbygget af bittesmå partikler. De kan ikke
Kemisk Reaktionslære ELO HARALD HANSEN. Polyteknisk Forlag. 2.udgave
 Kemisk Reaktionslære 2.udgave ELO HARALD HANSEN Polyteknisk Forlag Kemisk Reaktionslære Copyright 1984, 1987 by Elo Harald Hansen and Polyteknisk Forlag 1. udgave, 1. oplag 1984 2. udgave, 1. oplag 1987
Kemisk Reaktionslære 2.udgave ELO HARALD HANSEN Polyteknisk Forlag Kemisk Reaktionslære Copyright 1984, 1987 by Elo Harald Hansen and Polyteknisk Forlag 1. udgave, 1. oplag 1984 2. udgave, 1. oplag 1987
IONER OG SALTE. Et stabilt elektronsystem kan natrium- og chlor-atomerne også få, hvis de reagerer kemisk med hinanden:
 IONER OG SALTE INDLEDNING Når vi i daglig tale bruger udtrykket salt, mener vi altid køkkensalt, hvis kemiske navn er natriumchlorid, NaCl. Der findes imidlertid mange andre kemiske forbindelser, som er
IONER OG SALTE INDLEDNING Når vi i daglig tale bruger udtrykket salt, mener vi altid køkkensalt, hvis kemiske navn er natriumchlorid, NaCl. Der findes imidlertid mange andre kemiske forbindelser, som er
Et lident skrift til forståelse og oplysning om jernets molekylære LOGIK og skjønhed. Mads Jylov
 Et lident skrift til forståelse og oplysning om jernets molekylære LOGIK og skjønhed Mads Jylov Et lident skrift til forståelse og oplysning om jernets molekylære logik og skjønhed Copyright 2007 Mads
Et lident skrift til forståelse og oplysning om jernets molekylære LOGIK og skjønhed Mads Jylov Et lident skrift til forståelse og oplysning om jernets molekylære logik og skjønhed Copyright 2007 Mads
Røntgenstråling. Baggrund. Atomers struktur og Røntgenstråling
 Røntgenstråling Baggrund Bølgelængden af synligt lys ligger i området 400-750 nm. Ting med en mindre rumlig udstrækning kan vi ikke se med vores blotte øje. Det betyder, at hvis vi vil se på hvilke atomer
Røntgenstråling Baggrund Bølgelængden af synligt lys ligger i området 400-750 nm. Ting med en mindre rumlig udstrækning kan vi ikke se med vores blotte øje. Det betyder, at hvis vi vil se på hvilke atomer
Opgave: Du skal udfylde de manglende felter ud fra den information der er givet
 pgave 1a.01 Brug af det periodiske system pgave: Du skal udfylde de manglende felter ud fra den information der er givet Eks: I rubrik 1 kendte vi grundstof nummeret (nr. 11). Ved brug af det periodiske
pgave 1a.01 Brug af det periodiske system pgave: Du skal udfylde de manglende felter ud fra den information der er givet Eks: I rubrik 1 kendte vi grundstof nummeret (nr. 11). Ved brug af det periodiske
Atomer er betegnelsen for de kemisk mindste dele af grundstofferne.
 Atomets opbygning Atomer er betegnelsen for de kemisk mindste dele af grundstofferne. Guldatomet (kemiske betegnelse: Au) er f.eks. det mindst stykke metal, der stadig bærer navnet guld, det kan ikke yderlige
Atomets opbygning Atomer er betegnelsen for de kemisk mindste dele af grundstofferne. Guldatomet (kemiske betegnelse: Au) er f.eks. det mindst stykke metal, der stadig bærer navnet guld, det kan ikke yderlige
Varmebehandling af stål
 Varmebehandling af stål Stålets varmebehandling Når stål bliver udsat for plastisk deformation, spåntagende bearbejdning, støbning og svejsning, ændrer stålets struktur sig ofte på en sådan måde, at stålet
Varmebehandling af stål Stålets varmebehandling Når stål bliver udsat for plastisk deformation, spåntagende bearbejdning, støbning og svejsning, ændrer stålets struktur sig ofte på en sådan måde, at stålet
Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler
 Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler Antallet af protoner i atomkernen bestemmer navnet på atomet. Det uladede
Atomer består af: elektroner (negativ ladning), protoner (positiv ladning) kernepartikler neutroner (neutrale). kernepartikler Antallet af protoner i atomkernen bestemmer navnet på atomet. Det uladede
Hvilken betydning har legeringselementerne i stål, og hvordan kan legeringssammensætningen bestemmes?
 Hvilken betydning har legeringselementerne i stål, og hvordan kan legeringssammensætningen bestemmes? Af Carsten Jensen, FORCE Technology, Afdelingen for Korrosion & Metallurgi Risø-DTU, Roskilde, 24.
Hvilken betydning har legeringselementerne i stål, og hvordan kan legeringssammensætningen bestemmes? Af Carsten Jensen, FORCE Technology, Afdelingen for Korrosion & Metallurgi Risø-DTU, Roskilde, 24.
Naturfag for skov- og gartnerholdet
 Naturfag for skov- og gartnerholdet Grundlæggende kemi -Gennemgang af forskellige stoffers egenskaber og anvendelighed indenfor gartneri, anlægsgartneri og skovbrug 1 www.ucholstebro.dk. Døesvej 70 76.
Naturfag for skov- og gartnerholdet Grundlæggende kemi -Gennemgang af forskellige stoffers egenskaber og anvendelighed indenfor gartneri, anlægsgartneri og skovbrug 1 www.ucholstebro.dk. Døesvej 70 76.
Mikronæringsstoffer og Roedyrkning - vækst og sukkerindhold
 Københavns Universitet Saxkøbing, Vintermøde Roedyrkning: Mikronæringsstoffer og Roedyrkning - vækst og sukkerindhold Søren Husted, 5 Februar, 2019 Agenda: 9:35 10:15 De essentielle næringsstoffer og roedyrkning
Københavns Universitet Saxkøbing, Vintermøde Roedyrkning: Mikronæringsstoffer og Roedyrkning - vækst og sukkerindhold Søren Husted, 5 Februar, 2019 Agenda: 9:35 10:15 De essentielle næringsstoffer og roedyrkning
Nr. 6-2007 Grundstoffernes historie Fag: Fysik A/B/C Udarbejdet af: Michael Bjerring Christiansen, Århus Statsgymnasium, november 2008
 Nr. 6-007 Grundstoffernes historie Fag: Fysik A/B/C Udarbejdet af: Michael Bjerring Christiansen, Århus Statsgymnasium, november 008 Spørgsmål til artiklen. Hvilket grundstof, mente Hans Bethe, var det
Nr. 6-007 Grundstoffernes historie Fag: Fysik A/B/C Udarbejdet af: Michael Bjerring Christiansen, Århus Statsgymnasium, november 008 Spørgsmål til artiklen. Hvilket grundstof, mente Hans Bethe, var det
Forord 3. Udgave. Januar 2012 Jørgen Christoffersen
 Forord 3. Udgave Denne udgave er en lettere revidering af 2. udgave. Afsnittet om radioaktivitet er forbedret ved indsættelse af et appendiks. Jeg takker lektor, dr.phil. Niels Grunnet for hjælp til udarbejdelsen
Forord 3. Udgave Denne udgave er en lettere revidering af 2. udgave. Afsnittet om radioaktivitet er forbedret ved indsættelse af et appendiks. Jeg takker lektor, dr.phil. Niels Grunnet for hjælp til udarbejdelsen
Skriftlig prøve i kursus 26173/F14 Side 1 af 15 UORGANISK KEMI Torsdag den 22. maj 2014
 Skriftlig prøve i kursus 26173/F14 Side 1 af 15 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for He, Se, Cr 3+ og F. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Skriftlig prøve i kursus 26173/F14 Side 1 af 15 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for He, Se, Cr 3+ og F. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Materialer og Teknologi 1
 Materialer og Teknologi 1 Dagens program: Præsentation af kurset Præsentation af underviseren: Produktionsingeniør/Executive MBA (Henley) 16 års undervisningserfaring 14 års praktisk erfaring bl.a. med
Materialer og Teknologi 1 Dagens program: Præsentation af kurset Præsentation af underviseren: Produktionsingeniør/Executive MBA (Henley) 16 års undervisningserfaring 14 års praktisk erfaring bl.a. med
Skriftlig prøve i kursus 26173/E15 Side 1 af 14 UORGANISK KEMI Fredag den 18. december 2015
 Skriftlig prøve i kursus 26173/E15 Side 1 af 14 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for C, P, Zn 2+ og I. 2% 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Skriftlig prøve i kursus 26173/E15 Side 1 af 14 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for C, P, Zn 2+ og I. 2% 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Den kosmiske kalender
 Den kosmiske kalender JANUAR FEBRUAR MARTS APRIL MAJ JUNI AUGUST SEPTEMBER OKTOBER NOVEMBER DECEMBER Solsystemet Det første liv? Galakser JULI Eukaryoter DECEMBER 5 3 9 0 6 7 Den kambriske eksplosion 4
Den kosmiske kalender JANUAR FEBRUAR MARTS APRIL MAJ JUNI AUGUST SEPTEMBER OKTOBER NOVEMBER DECEMBER Solsystemet Det første liv? Galakser JULI Eukaryoter DECEMBER 5 3 9 0 6 7 Den kambriske eksplosion 4
Sporgrundstof definition:
 Forelæsning Sporgrundstoffer: fordeling, substitution og klassifikation Forelæsning: Hvad er et sporgrundstof? Grundstoffers elektronkonfiguration og radius Det Periodiske System Goldschmidts regler for
Forelæsning Sporgrundstoffer: fordeling, substitution og klassifikation Forelæsning: Hvad er et sporgrundstof? Grundstoffers elektronkonfiguration og radius Det Periodiske System Goldschmidts regler for
Platin komplekser i kampen mod kræft. Koordinationskemi i aktion. cis-ptcl 2 (NH 3 ) 2. Essentiel, nyttig eller toxisk. Hvad der faktisk skete
 Platin komplekser i kampen mod kræft et eksempel på Koordinationskemi i aktion Pt DNA DK 1 Har som den eneste vundet Tour de France syv gange (fra 1999 til 2005) Lance Armstrong blev vist født på en cykel
Platin komplekser i kampen mod kræft et eksempel på Koordinationskemi i aktion Pt DNA DK 1 Har som den eneste vundet Tour de France syv gange (fra 1999 til 2005) Lance Armstrong blev vist født på en cykel
Skriftlig prøve i kursus 26173/E14 Side 1 af 14 UORGANISK KEMI Fredag den 19. december 2014
 Skriftlig prøve i kursus 26173/E14 Side 1 af 14 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for O, Al, Fe 3+ og Br. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Skriftlig prøve i kursus 26173/E14 Side 1 af 14 Opgave 1. Molekylorbitalteori 1.1 Angiv elektronkonfigurationer for O, Al, Fe 3+ og Br. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for
Jordens skatte Ny Prisma Fysik og kemi 9 - kapitel 3 Skole: Navn: Klasse:
 Jordens skatte Ny Prisma Fysik og kemi 9 - kapitel 3 Skole: Navn: Klasse: Opgave 1 Et metal er kendetegnet ved, at nogle af metallets elektroner danner en elektrongas. Her er en række udsagn om, hvad et
Jordens skatte Ny Prisma Fysik og kemi 9 - kapitel 3 Skole: Navn: Klasse: Opgave 1 Et metal er kendetegnet ved, at nogle af metallets elektroner danner en elektrongas. Her er en række udsagn om, hvad et
Slibning af værktøjer til træindustrien
 Slibning af værktøjer til træindustrien Stållegeringer Stållegeringer, der anvendes i træindustrien: VS = værktøjsstål CV = krom-vanadiumstål HSS = hurtigstål HSSE = højlegeret hurtigstål HM = hårdmetal
Slibning af værktøjer til træindustrien Stållegeringer Stållegeringer, der anvendes i træindustrien: VS = værktøjsstål CV = krom-vanadiumstål HSS = hurtigstål HSSE = højlegeret hurtigstål HM = hårdmetal
Skriftlig prøve i kursus 26173/E12 Side 1 af 14 UORGANISK KEMI Tirsdag den 18. december 2012
 Skriftlig prøve i kursus 26173/E12 Side 1 af 14 Opgave 1. 1.1 Angiv elektronkonfigurationer for N, Al 3+, Mn og Zn 2+. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for Ne 2. 4 % b) Angiv
Skriftlig prøve i kursus 26173/E12 Side 1 af 14 Opgave 1. 1.1 Angiv elektronkonfigurationer for N, Al 3+, Mn og Zn 2+. 1.2 Molekylorbitalteori. a) Skitser molekylorbitaldiagrammet for Ne 2. 4 % b) Angiv
Sølvsmedeteknik. Før jeg vil beskrive sølvsmedeteknik vil jeg lige berette lidt om fagets historie.
 Sølvsmedeteknik Før jeg vil beskrive sølvsmedeteknik vil jeg lige berette lidt om fagets historie. Tidligere brugte man betegnelsen guld- og sølvsmed i flæng og et værksted fremstillede både smykker og
Sølvsmedeteknik Før jeg vil beskrive sølvsmedeteknik vil jeg lige berette lidt om fagets historie. Tidligere brugte man betegnelsen guld- og sølvsmed i flæng og et værksted fremstillede både smykker og
Lim mellem atomerne Ny Prisma Fysik og kemi 8. Skole: Navn: Klasse:
 Lim mellem atomerne Ny Prisma Fysik og kemi 8 Skole: Navn: Klasse: Opgave 1 Her ser du en modeltegning af et atom. Hvilket atom forestiller modellen? Der er 5 svarmuligheder. Sæt et kryds. Et oxygenatom
Lim mellem atomerne Ny Prisma Fysik og kemi 8 Skole: Navn: Klasse: Opgave 1 Her ser du en modeltegning af et atom. Hvilket atom forestiller modellen? Der er 5 svarmuligheder. Sæt et kryds. Et oxygenatom
Intra- og intermolekylære bindinger.
 Intra- og intermolekylære bindinger. Dipol-Dipol bindinger Londonbindinger ydrogen bindinger ydrofil ydrofob 1. Tilstandsformer... 1 2. Dipol-dipolbindinger... 2 3. Londonbindinger... 2 4. ydrogenbindinger....
Intra- og intermolekylære bindinger. Dipol-Dipol bindinger Londonbindinger ydrogen bindinger ydrofil ydrofob 1. Tilstandsformer... 1 2. Dipol-dipolbindinger... 2 3. Londonbindinger... 2 4. ydrogenbindinger....
Lokalenhed Midtjylland (MJL). Bilagsoversigt.
 Lokalenhed Midtjylland (MJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2
Lokalenhed Midtjylland (MJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2
Eksperimentelle øvelser, øvelse nummer 3 : Røntgenstråling målt med Ge-detektor
 Modtaget dato: (forbeholdt instruktor) Godkendt: Dato: Underskrift: Eksperimentelle øvelser, øvelse nummer 3 : Røntgenstråling målt med Ge-detektor Kristian Jerslev, Kristian Mads Egeris Nielsen, Mathias
Modtaget dato: (forbeholdt instruktor) Godkendt: Dato: Underskrift: Eksperimentelle øvelser, øvelse nummer 3 : Røntgenstråling målt med Ge-detektor Kristian Jerslev, Kristian Mads Egeris Nielsen, Mathias
Lokalenhed Storstrøm (STO). Bilagsoversigt.
 Lokalenhed Storstrøm (STO). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph Hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 )
Lokalenhed Storstrøm (STO). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph Hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 )
Navn Kemi opgaver Klasse 9. b Side 1 af 9. Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen sammen?
 Klasse 9. b Side 1 af 9 Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
Klasse 9. b Side 1 af 9 Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
Lokalenhed Østjylland (OJL). Bilagsoversigt.
 Lokalenhed Østjylland (OJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2
Lokalenhed Østjylland (OJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2
Lokalenhed Fyn (FYN). Bilagsoversigt.
 Lokalenhed Fyn (FYN). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 ) dybde
Lokalenhed Fyn (FYN). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 ) dybde
Lokalenhed Sjælland (SJL). Bilagsoversigt.
 Lokalenhed Sjælland (SJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 )
Lokalenhed Sjælland (SJL). Bilagsoversigt. ph-forhold ph dybde Bilag 1 Hydrogencarbonat (HCO 3 ) dybde Ca dybde ph hydrogencarbonat (HCO 3 ) ph Ca Redoxforhold Redoxpotentiale dybde Bilag 2 Ilt (O 2 )
Rådgivning ved revision af Bekendtgørelse nr. 637 Sammenstilling af analysekvalitet fra intern kvalitetskontrol
 Rådgivning ved revision af Bekendtgørelse nr. 637 Sammenstilling af analysekvalitet fra intern kvalitetskontrol Miljøstyrelsen Teknisk Notat Juni 2003 Sammenstilling af analysekvalitet fra intern kvalitetskontrol
Rådgivning ved revision af Bekendtgørelse nr. 637 Sammenstilling af analysekvalitet fra intern kvalitetskontrol Miljøstyrelsen Teknisk Notat Juni 2003 Sammenstilling af analysekvalitet fra intern kvalitetskontrol
GRUNDLÆGGENDE MATERIALELÆRE OG FORARBEJDNING 2. kursusgang
 GRUNDLÆGGENDE MATERIALELÆRE OG FORARBEJDNING 2. kursusgang GRUNDLÆGGENDE MATERIALELÆRE OG FORARBEJDNING Dagens emner: Repetition fra 1. kursusgang Atombindingstyper Interatomare kræfter Atompakning Metaller
GRUNDLÆGGENDE MATERIALELÆRE OG FORARBEJDNING 2. kursusgang GRUNDLÆGGENDE MATERIALELÆRE OG FORARBEJDNING Dagens emner: Repetition fra 1. kursusgang Atombindingstyper Interatomare kræfter Atompakning Metaller
I forløbet Atomet arbejdes med atomets opbygning. Forløbet består af 5 fagtekster, 31 opgaver og 8 aktiviteter. Derudover er der Videnstjek.
 Atomet Niveau: 8. klasse Varighed: 5 lektioner Præsentation: I forløbet Atomet arbejdes med atomets opbygning. Forløbet består af 5 fagtekster, 31 opgaver og 8 aktiviteter. Derudover er der Videnstjek.
Atomet Niveau: 8. klasse Varighed: 5 lektioner Præsentation: I forløbet Atomet arbejdes med atomets opbygning. Forløbet består af 5 fagtekster, 31 opgaver og 8 aktiviteter. Derudover er der Videnstjek.
Forelæsning 8. Stabile isotoper. Iltisotoper anvendt i paleoklimastudier, magmadannelse, termometri, vand-bjergart reaktion.
 Forelæsning: Hvad er stabile isotoper? Forelæsning 8 Stabile isotoper Fraktionering af stabile isotoper Iltisotoper Termometri Vand-bjergart reaktion Øvelse: Iltisotoper anvendt i paleoklimastudier, magmadannelse,
Forelæsning: Hvad er stabile isotoper? Forelæsning 8 Stabile isotoper Fraktionering af stabile isotoper Iltisotoper Termometri Vand-bjergart reaktion Øvelse: Iltisotoper anvendt i paleoklimastudier, magmadannelse,
Kemiske bindinger. Præsentation: Niveau: 8. klasse. Varighed: 7 lektioner
 Kemiske bindinger Niveau: 8. klasse Varighed: 7 lektioner Præsentation: Forløbet Kemiske bindinger omhandler ionbindinger, kovalente bindinger, metalbindinger, polære kovalente bindinger, hydrogenbindinger
Kemiske bindinger Niveau: 8. klasse Varighed: 7 lektioner Præsentation: Forløbet Kemiske bindinger omhandler ionbindinger, kovalente bindinger, metalbindinger, polære kovalente bindinger, hydrogenbindinger
Kemiske fingeraftryk af forureningsprofiler i jord nye analytiske redskaber til en differentieret risikovurdering
 Kemiske fingeraftryk af forureningsprofiler i jord nye analytiske redskaber til en differentieret risikovurdering Peter Mortensen, BU manager, Eurofins Miljø A/S Signe Vork, civilingeniør, Eurofins Miljø
Kemiske fingeraftryk af forureningsprofiler i jord nye analytiske redskaber til en differentieret risikovurdering Peter Mortensen, BU manager, Eurofins Miljø A/S Signe Vork, civilingeniør, Eurofins Miljø
Grundstofnavnenes oprindelse 2011
 Grundstofnavnenes oprindelse 2011 Nr. Symbol Dansk navn Engelsk navn Oprindelse 1 H Hydrogen (Brint) Hydrogen Gr. hydro, vand og genes, dannende 2 He Helium Helium Gr. helios, Solen 3 Li Lithium Lithium
Grundstofnavnenes oprindelse 2011 Nr. Symbol Dansk navn Engelsk navn Oprindelse 1 H Hydrogen (Brint) Hydrogen Gr. hydro, vand og genes, dannende 2 He Helium Helium Gr. helios, Solen 3 Li Lithium Lithium
Opgave. Navn Kemi opgaver Klasse Side 1 af 7. Hvad kaldes elementarpartiklerne, angiv deres ladning
 Klasse Side 1 af 7 Opgave Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
Klasse Side 1 af 7 Opgave Hvad kaldes elementarpartiklerne, angiv deres ladning Hvilke elementærpartikler frastøder hinanden i kernen? Hvilke elementærpartikler indeholder kærnekræfter, som holder kernen
A14 3 Magnetiske egenskaber
 A14 3 Magnetiske egenskaber Magnetiseringskurven De fleste af de ferro- og ferrimagnetiske stoffers magnetiske egenskaber kan aflæses af magnetiseringskurven, der er en graf som viser sammenhængen mellem
A14 3 Magnetiske egenskaber Magnetiseringskurven De fleste af de ferro- og ferrimagnetiske stoffers magnetiske egenskaber kan aflæses af magnetiseringskurven, der er en graf som viser sammenhængen mellem
A11 1 Elastisk og plastisk deformation Af Jørgen Bilde-Sørensen
 A11 1 Elastisk og plastisk deformation Af Jørgen Bilde-Sørensen Model til beregning af den kritiske forskydningsspænding Det kunne umiddelbart være nærliggende at forestille sig, at plastisk deformation
A11 1 Elastisk og plastisk deformation Af Jørgen Bilde-Sørensen Model til beregning af den kritiske forskydningsspænding Det kunne umiddelbart være nærliggende at forestille sig, at plastisk deformation
Støbejerns anvendelse, struktur og defekter
 Støbejerns anvendelse, struktur og defekter Kjell Wardenær, Senior Konsulent Elkem Nordic Bearbejdet for Støberiet af Herbert Wolthoorn Støbejern er en gruppe af jernlegeringer, der dækker et meget stort
Støbejerns anvendelse, struktur og defekter Kjell Wardenær, Senior Konsulent Elkem Nordic Bearbejdet for Støberiet af Herbert Wolthoorn Støbejern er en gruppe af jernlegeringer, der dækker et meget stort
Metallernes mikro- og makrostruktur
 Metallernes mikro- og makrostruktur Mikrostruktur Kim Metaller er sammensat af atomer. Forståelse for metallers opbygning gør det hensigtsmæssigt at betragte flydende metallers størkningsproces under deres
Metallernes mikro- og makrostruktur Mikrostruktur Kim Metaller er sammensat af atomer. Forståelse for metallers opbygning gør det hensigtsmæssigt at betragte flydende metallers størkningsproces under deres
maj 2017 Kemi C 326
 Nedenstående eksamensspørgsmål vil kunne trækkes ved eksaminationen af kursisterne på holdet KeC326. Hvis censor har indsigelser mod spørgsmålene, så kan der forekomme ændringer. Spørgsmål 1 + Spørgsmål
Nedenstående eksamensspørgsmål vil kunne trækkes ved eksaminationen af kursisterne på holdet KeC326. Hvis censor har indsigelser mod spørgsmålene, så kan der forekomme ændringer. Spørgsmål 1 + Spørgsmål
Salte, Syre og Baser
 Salte, Syre og Baser Fysik/Kemi Rapport 4/10 2011 MO Af Lukas Rønnow Klarlund 9.y Indholdsfortegnelse: Formål s. 2 Salte og Ioner s. 3 Syrer og Baser s. 5 phværdi s. 5 Neutralisation s. 6 Kunklusion s.
Salte, Syre og Baser Fysik/Kemi Rapport 4/10 2011 MO Af Lukas Rønnow Klarlund 9.y Indholdsfortegnelse: Formål s. 2 Salte og Ioner s. 3 Syrer og Baser s. 5 phværdi s. 5 Neutralisation s. 6 Kunklusion s.
En lille verden Ny Prisma Fysik og kemi 8. Skole: Navn: Klasse:
 En lille verden Ny Prisma Fysik og kemi 8 Skole: Navn: Klasse: For at løse nogle af opgaverne skal du benytte Nuklidtabel A og B på kopiark 6.4 og 6.5 i Kopimappe B, Ny Prisma 8. Opgave 1 Et atom består
En lille verden Ny Prisma Fysik og kemi 8 Skole: Navn: Klasse: For at løse nogle af opgaverne skal du benytte Nuklidtabel A og B på kopiark 6.4 og 6.5 i Kopimappe B, Ny Prisma 8. Opgave 1 Et atom består
Stålets legeringsstoffer
 Stålets legeringsstoffer Generelt De metaller, vi til daglig anvender i maskinindustrien, har mange forskellige egenskaber. Ser vi kun på f.eks. jern- og området, ved vi, at materialerne, når de skal bearbejdes,
Stålets legeringsstoffer Generelt De metaller, vi til daglig anvender i maskinindustrien, har mange forskellige egenskaber. Ser vi kun på f.eks. jern- og området, ved vi, at materialerne, når de skal bearbejdes,
Relativ massefylde. H3bli0102 Aalborg tekniske skole. Relativ massefylde H3bli0102 1
 Relativ massefylde H3bli0102 Aalborg tekniske skole Relativ massefylde H3bli0102 1 Indholdsfortegnelse Indholdsfortegnelse... Side 1 Formål... Side 2 Forsøget... Side 2- side 4 Konklusion... Side 4- side
Relativ massefylde H3bli0102 Aalborg tekniske skole Relativ massefylde H3bli0102 1 Indholdsfortegnelse Indholdsfortegnelse... Side 1 Formål... Side 2 Forsøget... Side 2- side 4 Konklusion... Side 4- side
Jordens salte Ny Prisma Fysik og kemi 9 - kapitel 2 Skole: Navn: Klasse:
 Jordens salte Ny Prisma Fysik og kemi 9 kapitel 2 Skole: Navn: Klasse: Opgave 1 I planternes blade foregår fotosyntesen, hvor planter forbruger vand og kuldioxid for bl.a. at danne oxygen. 6 H 2 O C 6
Jordens salte Ny Prisma Fysik og kemi 9 kapitel 2 Skole: Navn: Klasse: Opgave 1 I planternes blade foregår fotosyntesen, hvor planter forbruger vand og kuldioxid for bl.a. at danne oxygen. 6 H 2 O C 6
Side 1 Færøsk-Kapitel 74-141863 30/9/08
 Kapitel 74 KOBBER OG VARER DERAF Bestemmelse 1. I dette kapitel forstås ved: a)»raffineret kobber«metal, der indeholder mindst 99,85 vægtprocent kobber; eller metal, der indeholder mindst 97,5 vægtprocent
Kapitel 74 KOBBER OG VARER DERAF Bestemmelse 1. I dette kapitel forstås ved: a)»raffineret kobber«metal, der indeholder mindst 99,85 vægtprocent kobber; eller metal, der indeholder mindst 97,5 vægtprocent
GRUNDLÆGGENDE MATERIALELÆRE OG FORARBEJDNING 4. kursusgang
 GRUNDLÆGGENDE MATERIALELÆRE OG FORARBEJDNING 4. kursusgang GRUNDLÆGGENDE MATERIALELÆRE OG FORARBEJDNING Dagens emner: Repetition fra 3. kursusgang Teoretisk styrke Mikrostrukturelle påvirkninger Punktfejl
GRUNDLÆGGENDE MATERIALELÆRE OG FORARBEJDNING 4. kursusgang GRUNDLÆGGENDE MATERIALELÆRE OG FORARBEJDNING Dagens emner: Repetition fra 3. kursusgang Teoretisk styrke Mikrostrukturelle påvirkninger Punktfejl
Grundstoffer og det periodiske system
 Grundstoffer og det periodiske system Gør rede for atomets opbygning. Definer; atom, grundstof, isotop, molekyle, ion. Beskriv hvorfor de enkelte grundstoffer er placeret som de er i Det Periodiske System.
Grundstoffer og det periodiske system Gør rede for atomets opbygning. Definer; atom, grundstof, isotop, molekyle, ion. Beskriv hvorfor de enkelte grundstoffer er placeret som de er i Det Periodiske System.
Side 1 Færøsk-Kapitel 72-141863 30/9/08
 Kapitel 72 JERN OG STÅL Bestemmelser 1. I dette kapitel og for så vidt angår nedenstående punkt d, e og f overalt i nomenklaturen forstås ved nedenstående betegnelser følgende: a»råjern«legeringer af jern
Kapitel 72 JERN OG STÅL Bestemmelser 1. I dette kapitel og for så vidt angår nedenstående punkt d, e og f overalt i nomenklaturen forstås ved nedenstående betegnelser følgende: a»råjern«legeringer af jern
Fysik og kemi i 8. klasse
 Fysik og kemi i 8. klasse Teori til fysik- og kemiøvelserne ligger på nettet: fysik8.dk Udgivet af: Beskrivelser af elevforsøg Undervisningsforløb om atomfysik, mål & vægt, hverdagskemi, sæbe, metaller,
Fysik og kemi i 8. klasse Teori til fysik- og kemiøvelserne ligger på nettet: fysik8.dk Udgivet af: Beskrivelser af elevforsøg Undervisningsforløb om atomfysik, mål & vægt, hverdagskemi, sæbe, metaller,
Roden. Rodtyper Rodens opbygning og funktion Vandoptagelse og transport Næringsstofoptagelse og transport. Roden. Skiverod Hjerterod.
 Rodtyper s opbygning og funktion Vandoptagelse og transport Næringsstofoptagelse og transport Trævlerod Rodstængel Skiverod Hjerterod s funktion Fastholde planten Finde og optage vand Finde og optage næringsstoffer
Rodtyper s opbygning og funktion Vandoptagelse og transport Næringsstofoptagelse og transport Trævlerod Rodstængel Skiverod Hjerterod s funktion Fastholde planten Finde og optage vand Finde og optage næringsstoffer
Folkeskolens afgangsprøve Maj-juni 2006 Fysik / kemi - Facitliste
 Folkeskolens afgangsprøve Maj-juni 2006 1/25 Fk5 Opgave 1 / 20 (Opgaven tæller 5 %) I den atommodel, vi anvender i skolen, er et atom normalt opbygget af 3 forskellige partikler: elektroner, neutroner
Folkeskolens afgangsprøve Maj-juni 2006 1/25 Fk5 Opgave 1 / 20 (Opgaven tæller 5 %) I den atommodel, vi anvender i skolen, er et atom normalt opbygget af 3 forskellige partikler: elektroner, neutroner
Galvanisk Tæring. Kalium - mest negativ. Calsium
 Galvanisk Tæring Galvanisk tæring har også noget med El at gøre, idet det er elektronernes strøm, der forårsager, at de udfældede ioner i vandet søger hen til et negativt spændingspotentiale. Dette var
Galvanisk Tæring Galvanisk tæring har også noget med El at gøre, idet det er elektronernes strøm, der forårsager, at de udfældede ioner i vandet søger hen til et negativt spændingspotentiale. Dette var
Geokemisk differentiation af Jorden oversigt
 Forelæsning: Hvordan dannes magma Hvor dannes magma Forelæsning 9 Dannelse af magma Øvelse: Tryk og grad af opsmeltning; Sjældne jordarter (REE) som indikator for opsmeltningsbetingelser Hawai i F9 1 Geokemisk
Forelæsning: Hvordan dannes magma Hvor dannes magma Forelæsning 9 Dannelse af magma Øvelse: Tryk og grad af opsmeltning; Sjældne jordarter (REE) som indikator for opsmeltningsbetingelser Hawai i F9 1 Geokemisk
Partikler med fart på Ny Prisma Fysik og kemi 9 Skole: Navn: Klasse:
 Partikler med fart på Ny Prisma Fysik og kemi 9 Skole: Navn: Klasse: Opgave 1 Et atom har oftest to slags partikler i atomkernen. Hvad hedder partiklerne? Der er 6 linjer. Sæt et kryds ud for hver linje.
Partikler med fart på Ny Prisma Fysik og kemi 9 Skole: Navn: Klasse: Opgave 1 Et atom har oftest to slags partikler i atomkernen. Hvad hedder partiklerne? Der er 6 linjer. Sæt et kryds ud for hver linje.
Aluminium i levnedsmiddelindustrien Fremtidens metal?
 Aluminium i levnedsmiddelindustrien Fremtidens metal? v. Lektor, kemiingeniør Birgit Kjærside Storm Aalborg Universitet Esbjerg Roskilde 27.januar 2010 1 Aluminium Aluminium findes i store mængder i jordskorpen.
Aluminium i levnedsmiddelindustrien Fremtidens metal? v. Lektor, kemiingeniør Birgit Kjærside Storm Aalborg Universitet Esbjerg Roskilde 27.januar 2010 1 Aluminium Aluminium findes i store mængder i jordskorpen.
NATURFAG Fysik/kemi Folkeskolens afsluttende prøver Terminsprøve 2009/10
 NATURFAG Fysik/kemi Folkeskolens afsluttende prøver Terminsprøve 2009/10 Elevens navn: CPR-nr.: Skole: Klasse: Tilsynsførendes navn: 1 Tilstandsformer Tilstandsformer Opgave 1.1 Alle stoffer har 3 tilstandsformer.
NATURFAG Fysik/kemi Folkeskolens afsluttende prøver Terminsprøve 2009/10 Elevens navn: CPR-nr.: Skole: Klasse: Tilsynsførendes navn: 1 Tilstandsformer Tilstandsformer Opgave 1.1 Alle stoffer har 3 tilstandsformer.
Korrosion på affaldsanlæg
 Korrosion på affaldsanlæg Korrosion i forskellige miljøer Temadag på Haldor Topsøe d. 15. september Rikke Mattsson R&D Engineer Kort introduktion til Babcock & Wilcox Vølund Præsentation af et affaldsanlæg
Korrosion på affaldsanlæg Korrosion i forskellige miljøer Temadag på Haldor Topsøe d. 15. september Rikke Mattsson R&D Engineer Kort introduktion til Babcock & Wilcox Vølund Præsentation af et affaldsanlæg
10. juni 2016 Kemi C 325
 Grundstoffer og Det Periodiske System Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Forklar hvad der forstås med begrebet grundstoffer kontra kemiske forbindelser. Atomer er placeret
Grundstoffer og Det Periodiske System Spørgsmål 1 Forklar hvordan et atom er opbygget og hvad isotoper er. Forklar hvad der forstås med begrebet grundstoffer kontra kemiske forbindelser. Atomer er placeret
Gruppe 2 Læsestof : Kap. 11.
 ALKALIMETALLERNE Læsestof Inorganic Chemistry : Kap. 10, Kap 5.,afsnit 5.1-5.6 (incl.), 5.10- Øvelsesvejledning til Kemi C: s. 29-33 Spørgsmål: Hvordan forklarer vi normalpotentialernes uregelmæssige variation
ALKALIMETALLERNE Læsestof Inorganic Chemistry : Kap. 10, Kap 5.,afsnit 5.1-5.6 (incl.), 5.10- Øvelsesvejledning til Kemi C: s. 29-33 Spørgsmål: Hvordan forklarer vi normalpotentialernes uregelmæssige variation
Bilag 1: Kontrolprogram for Visse Vandværk
 Dok.nr.: 2018-025071-4 Revideret den 24-04-2018 Bilag 1: Kontrolprogram for Visse Vandværk Jupiter ID: 70206 Næste inspektion af rentvandstank: Ikke relevant Produceret/distribueret i 2017: 64.940/66.709
Dok.nr.: 2018-025071-4 Revideret den 24-04-2018 Bilag 1: Kontrolprogram for Visse Vandværk Jupiter ID: 70206 Næste inspektion af rentvandstank: Ikke relevant Produceret/distribueret i 2017: 64.940/66.709
( ) UDVIDET KONTROL + SPORSTOFKONTROL + ORGANISK MIKROFORURENING
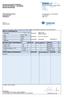 (03+08+09) UDVIDET KONTROL + SPORSTOFKONTROL + ORGANISK Vandværksvej 4 3450 Allerød Analyserapport nr. 20170202/005 22. april 2017 Blad 1 af 4 Kopi til: Jupiter (GEUS) Rapporten må kun gengives i uddrag,
(03+08+09) UDVIDET KONTROL + SPORSTOFKONTROL + ORGANISK Vandværksvej 4 3450 Allerød Analyserapport nr. 20170202/005 22. april 2017 Blad 1 af 4 Kopi til: Jupiter (GEUS) Rapporten må kun gengives i uddrag,
Valg af slibemiddel Til slibeskiver, der anvendes til slibning af værktøjer til træbearbejdning, kan slibemidlet være:
 Valg af slibemiddel Til slibeskiver, der anvendes til slibning af værktøjer til træbearbejdning, kan slibemidlet være: A = aluminiumoxid (elektrokorund) C = siliciumkarbid CBN = bornitrid D = naturlig
Valg af slibemiddel Til slibeskiver, der anvendes til slibning af værktøjer til træbearbejdning, kan slibemidlet være: A = aluminiumoxid (elektrokorund) C = siliciumkarbid CBN = bornitrid D = naturlig
Densitet (også kendt som massefylde og vægtfylde) hvor
 Nogle begreber: Densitet (også kendt som massefylde og vægtfylde) Molekylerne er tæt pakket: høj densitet Molekylerne er langt fra hinanden: lav densitet ρ = m V hvor ρ er densiteten m er massen Ver volumen
Nogle begreber: Densitet (også kendt som massefylde og vægtfylde) Molekylerne er tæt pakket: høj densitet Molekylerne er langt fra hinanden: lav densitet ρ = m V hvor ρ er densiteten m er massen Ver volumen
Galvanisk Tæring. med motoren. Man kan selvfølgelig også montere zinkanoden direkte på skrueakslen. Når man gør. Jens Koch
 Galvanisk Tæring med motoren. Man kan selvfølgelig også montere zinkanoden direkte på skrueakslen. Når man gør Jens Koch Galvanisk tæring har noget med el at gøre, idet det er elektronernes strøm der forårsager,
Galvanisk Tæring med motoren. Man kan selvfølgelig også montere zinkanoden direkte på skrueakslen. Når man gør Jens Koch Galvanisk tæring har noget med el at gøre, idet det er elektronernes strøm der forårsager,
Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse:
 Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse: Opgave 1 Den kemiske formel for køkkensalt er NaCl. Her er en række udsagn om køkkensalt. Sæt kryds ved sandt
Det sure, det salte, det basiske Ny Prisma Fysik og kemi 9 - kapitel 1 Skole: Navn: Klasse: Opgave 1 Den kemiske formel for køkkensalt er NaCl. Her er en række udsagn om køkkensalt. Sæt kryds ved sandt
(03+09) UDVIDET KONTROL + ORGANISK MIKROFORURENING
 Vandværksvej 4 3450 Allerød Analyserapport nr. 20160205/012 16. februar 2016 Blad 1 af 5 Kopi til: Jupiter (GEUS) Rapporten må kun gengives i uddrag, hvis laboratoriet har godkendt uddraget. Resultatet
Vandværksvej 4 3450 Allerød Analyserapport nr. 20160205/012 16. februar 2016 Blad 1 af 5 Kopi til: Jupiter (GEUS) Rapporten må kun gengives i uddrag, hvis laboratoriet har godkendt uddraget. Resultatet
Hvor mange neutroner og protoner er der i plutonium-isotopen
 Atomet Tjek din viden om atomet. 3.1 4.1 Atommasse måles i Skriv navnene på partiklerne i atomet. Hvad angiver tallene i den kernefysiske skrivemåde? 4 2 He 13 6 Tegn atomkernen til kulstof-isotopen C.
Atomet Tjek din viden om atomet. 3.1 4.1 Atommasse måles i Skriv navnene på partiklerne i atomet. Hvad angiver tallene i den kernefysiske skrivemåde? 4 2 He 13 6 Tegn atomkernen til kulstof-isotopen C.
Kernereaktioner. 1 Energi og masse
 Kernereaktioner 7 1 Energi og masse Ifølge relativitetsteorien gælder det, at når der tilføres energi til et system, vil systemets masse altid vokse. Sammenhængen mellem energitilvæksten og massetilvækstener
Kernereaktioner 7 1 Energi og masse Ifølge relativitetsteorien gælder det, at når der tilføres energi til et system, vil systemets masse altid vokse. Sammenhængen mellem energitilvæksten og massetilvækstener
Syrer, baser og salte:
 Syrer, baser og salte: Salte: Salte er en stor gruppe af kemiske stoffer med en række fælles egenskaber I tør, fast form er de krystaller. Opløst i vand danner de frie ioner som giver vandet elektrisk
Syrer, baser og salte: Salte: Salte er en stor gruppe af kemiske stoffer med en række fælles egenskaber I tør, fast form er de krystaller. Opløst i vand danner de frie ioner som giver vandet elektrisk
Forsøg med magneter (permanente magneter)
 Forsøg med magneter (permanente magneter) Hvis der ikke er plads nok til notater her på papiret, så lav tegninger, forklaringer og noter resultater i dit hæfte. 1. Læg en magnet på et stykke flamingoplade
Forsøg med magneter (permanente magneter) Hvis der ikke er plads nok til notater her på papiret, så lav tegninger, forklaringer og noter resultater i dit hæfte. 1. Læg en magnet på et stykke flamingoplade
Efteruddannelse i Materialeteknologi Kursus S1/ A. Materialekendskab. Stål generelt
 Efteruddannelse i Materialeteknologi Kursus S1/ A Materialekendskab Stål generelt Kursusmateriale udviklet under lov 271 om efteruddannels e i et samarbejde melle m Danmarks Ingeniørakademi, Teknologisk
Efteruddannelse i Materialeteknologi Kursus S1/ A Materialekendskab Stål generelt Kursusmateriale udviklet under lov 271 om efteruddannels e i et samarbejde melle m Danmarks Ingeniørakademi, Teknologisk
HVAD ER RADIOAKTIV STRÅLING
 16. Radioaktiv stråling kaldes i videnskabelige kredse Joniserende stråling Stråling som påvirker alt stof ved at danne joner, som er elektrisk ladede atomer eller molekyler. Joniserende stråling skader
16. Radioaktiv stråling kaldes i videnskabelige kredse Joniserende stråling Stråling som påvirker alt stof ved at danne joner, som er elektrisk ladede atomer eller molekyler. Joniserende stråling skader
Økologi kemisk fingerprinting
 Konference om fødevareautencitet: Mg P K B Mn S Cl Cu Zn Fe Ca Mo Ni 0 50 100 150 200 250 Mass (m/z) Økologi kemisk fingerprinting Søren Husted, Institut for Jordbrug og Økologi, IJØ, Det Biovidenskabelige
Konference om fødevareautencitet: Mg P K B Mn S Cl Cu Zn Fe Ca Mo Ni 0 50 100 150 200 250 Mass (m/z) Økologi kemisk fingerprinting Søren Husted, Institut for Jordbrug og Økologi, IJØ, Det Biovidenskabelige
MEDDELELSE FRA KOMMISSIONEN TIL EUROPA-PARLAMENTET, RÅDET, DET EUROPÆISKE ØKONOMISKE OG SOCIALE UDVALG OG REGIONSUDVALGET
 EUROPA- KOMMISSIONEN Bruxelles, den 13.9.2017 COM(2017) 490 final MEDDELELSE FRA KOMMISSIONEN TIL EUROPA-PARLAMENTET, RÅDET, DET EUROPÆISKE ØKONOMISKE OG SOCIALE UDVALG OG REGIONSUDVALGET om 2017-listen
EUROPA- KOMMISSIONEN Bruxelles, den 13.9.2017 COM(2017) 490 final MEDDELELSE FRA KOMMISSIONEN TIL EUROPA-PARLAMENTET, RÅDET, DET EUROPÆISKE ØKONOMISKE OG SOCIALE UDVALG OG REGIONSUDVALGET om 2017-listen
Torben Rosenørn. Aalborg Universitet. Campus Esbjerg
 Torben Rosenørn Aalborg Universitet Campus Esbjerg 1 Definition af syrer En syre er et stof som kan fraspalte en proton (H + ). H + optræder i vand sammen med et vandmolekyle (H 2 O) som H 3 O + Syrer
Torben Rosenørn Aalborg Universitet Campus Esbjerg 1 Definition af syrer En syre er et stof som kan fraspalte en proton (H + ). H + optræder i vand sammen med et vandmolekyle (H 2 O) som H 3 O + Syrer
Korrosion i praksis. Troels Mathiesen. Afdelingen for Korrosion og Metallurgi trm@force.dk
 Korrosion i praksis Troels Mathiesen Specialist, civ.ing., ph.d. Afdelingen for Korrosion og Metallurgi trm@force.dk Kundeopgaver: 50% Skadesopklaring 50% Rådgivning, korrosionstest, R&D Specialer: rustfrit
Korrosion i praksis Troels Mathiesen Specialist, civ.ing., ph.d. Afdelingen for Korrosion og Metallurgi trm@force.dk Kundeopgaver: 50% Skadesopklaring 50% Rådgivning, korrosionstest, R&D Specialer: rustfrit
Gødningslære A. Faglærer Karin Juul Hesselsøe
 Faglærer Karin Juul Hesselsøe Gødningslære er enkelt Gødningslære er enkelt For lidt Gødningslære er enkelt Alt for meget Det kan være svært at finde balancen Planter består mest af sukkerstoffer Kulhydrater
Faglærer Karin Juul Hesselsøe Gødningslære er enkelt Gødningslære er enkelt For lidt Gødningslære er enkelt Alt for meget Det kan være svært at finde balancen Planter består mest af sukkerstoffer Kulhydrater
Guldbog Kemi C Copyright 2016 af Mira Backes og Christian Bøgelund.
 Guldbog Kemi C Copyright 2016 af Mira Backes og Christian Bøgelund. Alle rettigheder forbeholdes. Mekanisk, fotografisk eller elektronisk gengivelse af denne bog eller dele heraf er uden forfatternes skriftlige
Guldbog Kemi C Copyright 2016 af Mira Backes og Christian Bøgelund. Alle rettigheder forbeholdes. Mekanisk, fotografisk eller elektronisk gengivelse af denne bog eller dele heraf er uden forfatternes skriftlige
Kontrol af gødning 2018 Oversigt over analyseresultater. Juni 2018
 Kontrol af gødning 2018 Oversigt over analyseresultater Juni 2018 Kolofon Kontrol af gødning 2018 Oversigt over analyseresultater Denne offentliggørelse er udarbejdet af Miljø- og Fødevareministeriet i
Kontrol af gødning 2018 Oversigt over analyseresultater Juni 2018 Kolofon Kontrol af gødning 2018 Oversigt over analyseresultater Denne offentliggørelse er udarbejdet af Miljø- og Fødevareministeriet i
Kontrol af gødning 2017 Oversigt over analyseresultater. December 2017
 Kontrol af gødning 2017 Oversigt over analyseresultater December 2017 Kolofon Kontrol af gødning 2017 Oversigt over analyseresultater Denne offentliggørelse er udarbejdet af Miljø- og Fødevareministeriet
Kontrol af gødning 2017 Oversigt over analyseresultater December 2017 Kolofon Kontrol af gødning 2017 Oversigt over analyseresultater Denne offentliggørelse er udarbejdet af Miljø- og Fødevareministeriet
AB. SVEJSETEKNIK ApS.
 AB 1770 AC-DC Med den nye Dual Flow coatning er det kun nødvendigt at svejse 2/3 af godstykkelsen. Støbejern. Støbejern bruges meget i industrien på grund af prisen, samt at det er et stabilt og bearbejdeligt
AB 1770 AC-DC Med den nye Dual Flow coatning er det kun nødvendigt at svejse 2/3 af godstykkelsen. Støbejern. Støbejern bruges meget i industrien på grund af prisen, samt at det er et stabilt og bearbejdeligt
Hvad er rustfrit? i 1. Rustfrit stål
 Hvad er rustfrit? i 1 Rustfrit stål Rustfrit stål er en fælles betegnelse for en mængde stål med den fællesnævner, at de indeholder mindst 11,5% chrom. Når jern legeres med mindst 11,5% chrom, reagerer
Hvad er rustfrit? i 1 Rustfrit stål Rustfrit stål er en fælles betegnelse for en mængde stål med den fællesnævner, at de indeholder mindst 11,5% chrom. Når jern legeres med mindst 11,5% chrom, reagerer
Metallernes kemi. Præsentation: Niveau: 8. klasse. Varighed: 6 lektioner
 Metallernes kemi Niveau: 8. klasse Varighed: 6 lektioner Præsentation: Forløbet Metallernes kemi er placeret i fysik-kemifokus.dk 8. klasse, og det bygger på viden fra forløbene Atomer og molekyler, Atomet
Metallernes kemi Niveau: 8. klasse Varighed: 6 lektioner Præsentation: Forløbet Metallernes kemi er placeret i fysik-kemifokus.dk 8. klasse, og det bygger på viden fra forløbene Atomer og molekyler, Atomet
Kontrol af gødning 2018 Oversigt over analyseresultater
 Kontrol af gødning 2018 Oversigt over analyseresultater Juli 2018 Kontrol af gødning 2018 Oversigt over analyseresultater Denne vejledning er udarbejdet af Landbrugsstyrelsen i 2018 Landbrugsstyrelsen
Kontrol af gødning 2018 Oversigt over analyseresultater Juli 2018 Kontrol af gødning 2018 Oversigt over analyseresultater Denne vejledning er udarbejdet af Landbrugsstyrelsen i 2018 Landbrugsstyrelsen
Definition af base (Brøndsted): En base er et molekyle eller en jon, der kan optage en hydron. En hydron er en H +
 Definition af base (Brøndsted): En base er et molekyle eller en jon, der kan optage en hydron En hydron er en H + Ved en syrebasereaktion overføres der en hydron fra en syre til en base En syre indeholder
Definition af base (Brøndsted): En base er et molekyle eller en jon, der kan optage en hydron En hydron er en H + Ved en syrebasereaktion overføres der en hydron fra en syre til en base En syre indeholder
Fysikforløb nr. 6. Atomfysik
 Fysikforløb nr. 6. Atomfysik I uge 8 begynder vi på atomfysik. Derfor får du dette kompendie, så du i god tid, kan begynde, at forberede dig på emnet. Ideen med dette kompendie er også, at du her får en
Fysikforløb nr. 6. Atomfysik I uge 8 begynder vi på atomfysik. Derfor får du dette kompendie, så du i god tid, kan begynde, at forberede dig på emnet. Ideen med dette kompendie er også, at du her får en
NOTAT. 1. Indledning. Jf. vilkår 33 i miljøgodkendelsen /1/ skal der desuden foretages monitering og egenkontrol af følgende parametre uden kravværdi:
 NOTAT Projekt Ll. Torup Gaslager Egenkontrol (metaller, susp. stof mv.) Kunde Energinet.dk Notat nr. Egenkontrol nr. 3 (rev. 1) Dato 01-09-2015 Til Fra Miljøstyrelsen og Energinet.dk Rambøll 1. Indledning
NOTAT Projekt Ll. Torup Gaslager Egenkontrol (metaller, susp. stof mv.) Kunde Energinet.dk Notat nr. Egenkontrol nr. 3 (rev. 1) Dato 01-09-2015 Til Fra Miljøstyrelsen og Energinet.dk Rambøll 1. Indledning
